Het arrangement Thema: Antibiotica vwo456 is gemaakt met Wikiwijs van Kennisnet. Wikiwijs is hét onderwijsplatform waar je leermiddelen zoekt, maakt en deelt.
- Auteur
- Laatst gewijzigd
- 21-01-2025 19:59:32
- Licentie
-
Dit lesmateriaal is gepubliceerd onder de Creative Commons Naamsvermelding-GelijkDelen 4.0 Internationale licentie. Dit houdt in dat je onder de voorwaarde van naamsvermelding en publicatie onder dezelfde licentie vrij bent om:
- het werk te delen - te kopiëren, te verspreiden en door te geven via elk medium of bestandsformaat
- het werk te bewerken - te remixen, te veranderen en afgeleide werken te maken
- voor alle doeleinden, inclusief commerciële doeleinden.
Meer informatie over de CC Naamsvermelding-GelijkDelen 4.0 Internationale licentie.
Colofon
De module Antibiotica om ons heen is ontwikkeld door medewerkers van StudioVO.
Fair Use
In de Stercollecties van StudioVO wordt gebruik gemaakt van beeld- en filmmateriaal dat beschikbaar is op het internet. Bij het gebruik zijn we uitgegaan van fair use.
Meer informatie: Fair use .
Mocht u vragen/opmerkingen hebben,
neem dan contact op via de helpdesk VO-Content .
Aanvullende informatie over dit lesmateriaal
Van dit lesmateriaal is de volgende aanvullende informatie beschikbaar:
- Toelichting
- Dit thema valt onder de arrangeerbare leerlijn van de Stercollecties voor scheikunde voor vwo leerjaar 456. De volgende onderdelen worden behandeld: antibiotica. De student gebruikt de opgedane kennis in deze verwerkingsles.
- Leerniveau
- VWO 6; VWO 4; VWO 5;
- Leerinhoud en doelen
- Scheikunde; Reactiviteit; Chemische processen;
- Eindgebruiker
- leerling/student
- Moeilijkheidsgraad
- gemiddeld
- Studiebelasting
- 10 uur 0 minuten
- Trefwoorden
- aminozuur, antibiotica, arrangeerbaar, bacterien, enzym, scheikunde, stercollectie, vwo 456

 Je hebt vast wel eens een antibioticakuur gehad.
Je hebt vast wel eens een antibioticakuur gehad. Wat ga ik doen?
Wat ga ik doen?

 Stap 1:
Stap 1:  Stap 2:
Stap 2:  Stap 3:
Stap 3:  Stap 4:
Stap 4:  Stap 5:
Stap 5: 

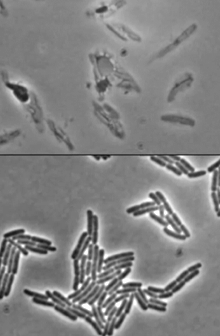
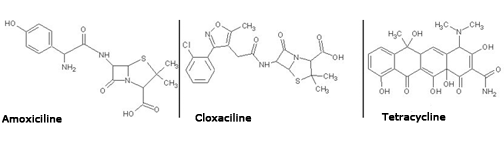 04 - individueel
04 - individueel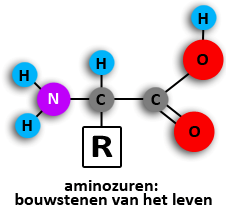


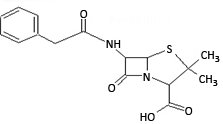
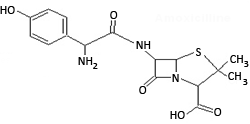
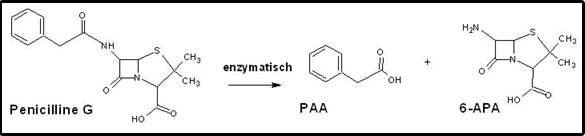
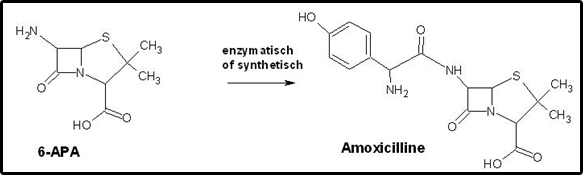

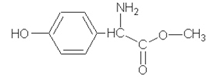 Dit is een ester. Welk alcohol (naam geven) splitst zich af bij hydrolyse?
Dit is een ester. Welk alcohol (naam geven) splitst zich af bij hydrolyse?
 Stap 2 - Enzym uit de bron halen
Stap 2 - Enzym uit de bron halen