Het arrangement Atoom vmbo234 is gemaakt met Wikiwijs van Kennisnet. Wikiwijs is hét onderwijsplatform waar je leermiddelen zoekt, maakt en deelt.
- Auteur
- Laatst gewijzigd
- 21-01-2025 17:27:51
- Licentie
-
Dit lesmateriaal is gepubliceerd onder de Creative Commons Naamsvermelding-GelijkDelen 4.0 Internationale licentie. Dit houdt in dat je onder de voorwaarde van naamsvermelding en publicatie onder dezelfde licentie vrij bent om:
- het werk te delen - te kopiëren, te verspreiden en door te geven via elk medium of bestandsformaat
- het werk te bewerken - te remixen, te veranderen en afgeleide werken te maken
- voor alle doeleinden, inclusief commerciële doeleinden.
Meer informatie over de CC Naamsvermelding-GelijkDelen 4.0 Internationale licentie.
Aanvullende informatie over dit lesmateriaal
Van dit lesmateriaal is de volgende aanvullende informatie beschikbaar:
- Toelichting
- Deze les valt onder de arrangeerbare leerlijn van de Stercollectie voor NaSk voor vmbo leerjaar2/ 3/4. Dit is thema ’Verbranding en energie'. Het onderwerp van deze les is: atoom. Je leert beschrijven dat een molecuul het kleinste deeltje is dat nog de eigenschappen van een stof heeft en is opgebouwd uit atomen, een zuivere stof en een mengsel op deeltjesniveau beschrijven met een tekening, de verschillende fasen van stoffen op deeltjesniveau beschrijven met een tekening.
- Leerniveau
- VMBO gemengde leerweg, 2; VMBO kaderberoepsgerichte leerweg, 2; VMBO gemengde leerweg, 3; VMBO theoretische leerweg, 4; VMBO theoretische leerweg, 2; VMBO theoretische leerweg, 3; VMBO kaderberoepsgerichte leerweg, 4; VMBO gemengde leerweg, 4; VMBO kaderberoepsgerichte leerweg, 3;
- Leerinhoud en doelen
- Materie; NaSk; Chemische reacties; Natuurkunde;
- Eindgebruiker
- leerling/student
- Moeilijkheidsgraad
- gemiddeld
- Studiebelasting
- 4 uur 0 minuten
- Trefwoorden
- arrangeerbaar, atoom, deeltjesniveau, fasen van stoffen, mengsel, molecuul, nask, stercollectie, vmbo2/3/4


 John Dalton (1766 – 1844)
John Dalton (1766 – 1844) Leerdoelen
Leerdoelen


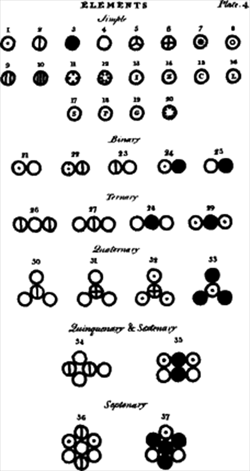 Je gaat een stuk lezen van het boek “A New System of Chemical Philosophy” van John Dalton. De tekst is vanuit het Engels in het Nederlands vertaald en enigszins vereenvoudigd.
Je gaat een stuk lezen van het boek “A New System of Chemical Philosophy” van John Dalton. De tekst is vanuit het Engels in het Nederlands vertaald en enigszins vereenvoudigd. Ga ervan uit dat de theorie van Dalton klopt.
Ga ervan uit dat de theorie van Dalton klopt. De bouwstenen van stoffen zijn moleculen. Moleculen kunnen bestaan uit één of meerdere atomen. Moleculen zijn dus de kleinste bouwstenen die de eigenschappen van een stof bepalen.
De bouwstenen van stoffen zijn moleculen. Moleculen kunnen bestaan uit één of meerdere atomen. Moleculen zijn dus de kleinste bouwstenen die de eigenschappen van een stof bepalen.


