Het arrangement Thema: Kolenvergasser vwo456 is gemaakt met Wikiwijs van Kennisnet. Wikiwijs is hét onderwijsplatform waar je leermiddelen zoekt, maakt en deelt.
- Auteur
- Laatst gewijzigd
- 21-01-2025 20:05:21
- Licentie
-
Dit lesmateriaal is gepubliceerd onder de Creative Commons Naamsvermelding-GelijkDelen 4.0 Internationale licentie. Dit houdt in dat je onder de voorwaarde van naamsvermelding en publicatie onder dezelfde licentie vrij bent om:
- het werk te delen - te kopiëren, te verspreiden en door te geven via elk medium of bestandsformaat
- het werk te bewerken - te remixen, te veranderen en afgeleide werken te maken
- voor alle doeleinden, inclusief commerciële doeleinden.
Meer informatie over de CC Naamsvermelding-GelijkDelen 4.0 Internationale licentie.
Colofon
De module Kolenvergasser is ontwikkeld door Sander Bons en medewerkers van StudioVO op basis van materiaal van xxxxxxxxxxxxxxxxxx.
Bij het ontwikkelen van het materiaal is gebruik gemaakt van of wordt verwezen naar materiaal van de volgende websites:
Fair Use
In de Stercollecties van StudioVO wordt gebruik gemaakt van beeld- en filmmateriaal dat beschikbaar is op het internet. Bij het gebruik zijn we uitgegaan van fair use.
Meer informatie: Fair use.
Mocht u vragen/opmerkingen hebben,
neem dan contact op via de helpdesk VO-Content.
Aanvullende informatie over dit lesmateriaal
Van dit lesmateriaal is de volgende aanvullende informatie beschikbaar:
- Toelichting
- Dit thema valt onder de arrangeerbare leerlijn van de Stercollecties voor scheikunde voor vwo leerjaar 456. Energieproducent NUON heeft in de Eemshaven een kolencentrale gebouwd. Deze centrale voorziet maar liefst 2 miljoen Nederlandse huishoudens van stroom. In deze module nemen we een kijkje in deze centrale.
- Leerniveau
- VWO 6; VWO 4; VWO 5;
- Leerinhoud en doelen
- Scheikunde; Systeemdenken (scheikunde); Duurzaamheid;
- Eindgebruiker
- leerling/student
- Moeilijkheidsgraad
- gemiddeld
- Studiebelasting
- 12 uur 0 minuten
- Trefwoorden
- arrangeerbaar, co2, energie, kolencentrale, reactor, scheikunde, stercollectie, stroom, vwo 456

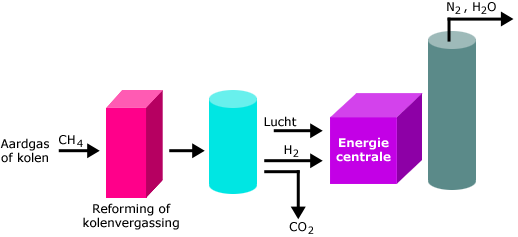
 Energieproducent NUON heeft in de Eemshaven een kolencentrale gebouwd. Deze centrale voorziet maar liefst 2 miljoen Nederlandse huishoudens van stroom.
Energieproducent NUON heeft in de Eemshaven een kolencentrale gebouwd. Deze centrale voorziet maar liefst 2 miljoen Nederlandse huishoudens van stroom.





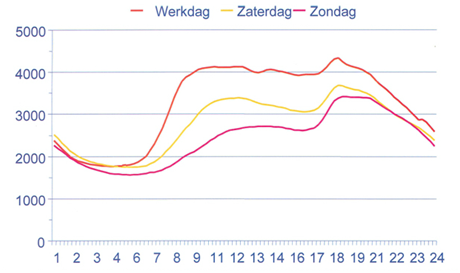






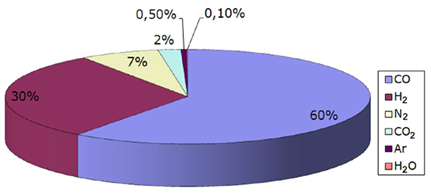
 Bekijk nu de afbeelding hiernaast.
Bekijk nu de afbeelding hiernaast.







 Benodigdheden
Benodigdheden