Het arrangement Thema: Parfum vwo456 is gemaakt met Wikiwijs van Kennisnet. Wikiwijs is hét onderwijsplatform waar je leermiddelen zoekt, maakt en deelt.
- Auteur
- Laatst gewijzigd
- 21-01-2025 20:09:37
- Licentie
-
Dit lesmateriaal is gepubliceerd onder de Creative Commons Naamsvermelding-GelijkDelen 4.0 Internationale licentie. Dit houdt in dat je onder de voorwaarde van naamsvermelding en publicatie onder dezelfde licentie vrij bent om:
- het werk te delen - te kopiëren, te verspreiden en door te geven via elk medium of bestandsformaat
- het werk te bewerken - te remixen, te veranderen en afgeleide werken te maken
- voor alle doeleinden, inclusief commerciële doeleinden.
Meer informatie over de CC Naamsvermelding-GelijkDelen 4.0 Internationale licentie.
StudioVO
Deze module is ontwikkeld door medewerkers van StudioVO.
Fair Use
In de Stercollecties van StudioVO wordt gebruik gemaakt van beeld- en filmmateriaal dat beschikbaar is op internet. Bij het gebruik zijn we uitgegaan van fair use. Meer informatie: Fair use
Mocht u vragen/opmerkingen hebben, neem dan contact op via de helpdesk VO-content.
Aanvullende informatie over dit lesmateriaal
Van dit lesmateriaal is de volgende aanvullende informatie beschikbaar:
- Leerniveau
- VWO 6; VWO 4; VWO 5;
- Leerinhoud en doelen
- Scheikunde; Reactiviteit; Productieprocessen;
- Eindgebruiker
- leerling/student
- Moeilijkheidsgraad
- gemiddeld
- Studiebelasting
- 19 uur 0 minuten
- Trefwoorden
- arrangeerbaar, arrangeerbare, leerlijn, rearrangeerbare











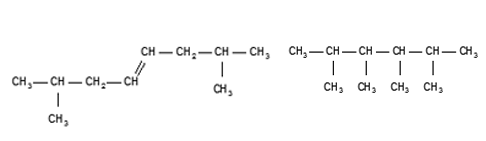

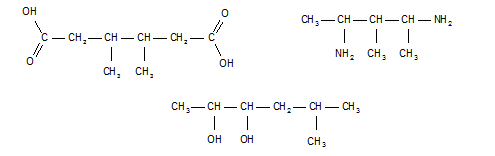

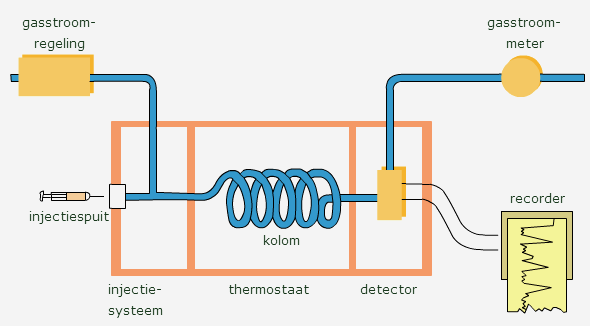
 Gaschromatografie lijkt veel op papierchromatografie: de kolom is vergelijkbaar met het papier, het dragergas met de loopvloeistof. Het verschil is dat bij de gaschromatograaf alle stoffen erdoorheen komen. Bij papierchromatografie blijven stoffen aan het papier hangen. In een specifieke vorm van gaschromatografie berust de scheiding op molecuulgrootte: grotere moleculen kunnen de kolom minder makkelijk passeren (worden meer tegengehouden) dan kleinere moleculen.
Gaschromatografie lijkt veel op papierchromatografie: de kolom is vergelijkbaar met het papier, het dragergas met de loopvloeistof. Het verschil is dat bij de gaschromatograaf alle stoffen erdoorheen komen. Bij papierchromatografie blijven stoffen aan het papier hangen. In een specifieke vorm van gaschromatografie berust de scheiding op molecuulgrootte: grotere moleculen kunnen de kolom minder makkelijk passeren (worden meer tegengehouden) dan kleinere moleculen.




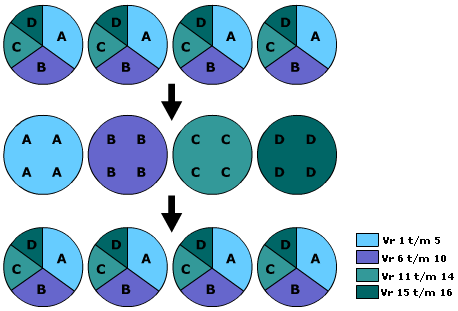 Elke groep bestaat uit vier leerlingen. Elke leerling (a, b, c en d) beantwoord zijn eigen vragen.
Elke groep bestaat uit vier leerlingen. Elke leerling (a, b, c en d) beantwoord zijn eigen vragen.





