Het arrangement Bepaling van het fosfaatgehalte van wasmiddelen is gemaakt met Wikiwijs van Kennisnet. Wikiwijs is hét onderwijsplatform waar je leermiddelen zoekt, maakt en deelt.
- Auteurs
- Laatst gewijzigd
- 06-10-2015 20:46:44
- Licentie
-
Dit lesmateriaal is gepubliceerd onder de Creative Commons Naamsvermelding 3.0 Nederlands licentie. Dit houdt in dat je onder de voorwaarde van naamsvermelding vrij bent om:
- het werk te delen - te kopiëren, te verspreiden en door te geven via elk medium of bestandsformaat
- het werk te bewerken - te remixen, te veranderen en afgeleide werken te maken
- voor alle doeleinden, inclusief commerciële doeleinden.
Meer informatie over de CC Naamsvermelding 3.0 Nederland licentie.
Aanvullende informatie over dit lesmateriaal
Van dit lesmateriaal is de volgende aanvullende informatie beschikbaar:
- Toelichting
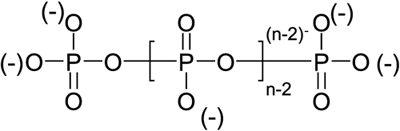
- Wasmiddelen bevatten vaak polyfosfaten. Polyfosfaten ontharden het water, waardoor de waseigenschap van het wasmiddel verbetert. In dit arrangement wordt beschreven hoe het fosfaatgehalte van een wasmiddel kan worden bepaald via colorimetrie, zowel visueel als met een spectrofotometer.
- Leerniveau
- HAVO 4; VWO 6; HBO; HAVO 5; HBO - Master; VWO 5; HBO - Bachelor;
- Leerinhoud en doelen
- Scheikunde;
- Eindgebruiker
- leraar
- Moeilijkheidsgraad
- gemiddeld
- Studiebelasting
- 0 uur 50 minuten
- Trefwoorden
- analysetechnieken, antikalk, colorimeter, fosfaat, fosfaatgehalte, onderzoeksvaardigheden, polyfosfaat, ris-publicatie, ris-publicatie vii, technisch-instrumentele vaardigheden, wasmiddel, wasmiddelen