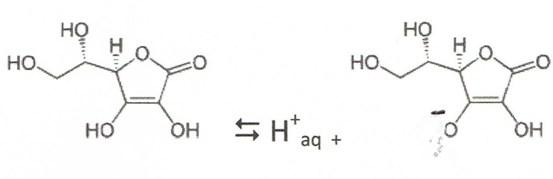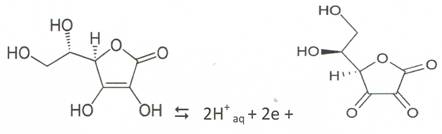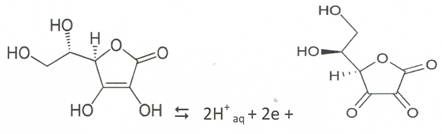Het arrangement Bepaling van het vitamine C-gehalte is gemaakt met Wikiwijs van Kennisnet. Wikiwijs is hét onderwijsplatform waar je leermiddelen zoekt, maakt en deelt.
- Auteur
- Laatst gewijzigd
- 17-06-2021 13:48:48
- Licentie
-
Dit lesmateriaal is gepubliceerd onder de Creative Commons Naamsvermelding 3.0 Nederlands licentie. Dit houdt in dat je onder de voorwaarde van naamsvermelding vrij bent om:
- het werk te delen - te kopiëren, te verspreiden en door te geven via elk medium of bestandsformaat
- het werk te bewerken - te remixen, te veranderen en afgeleide werken te maken
- voor alle doeleinden, inclusief commerciële doeleinden.
Meer informatie over de CC Naamsvermelding 3.0 Nederland licentie.
Aanvullende informatie over dit lesmateriaal
Van dit lesmateriaal is de volgende aanvullende informatie beschikbaar:
- Toelichting
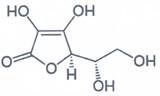
- Het vitamine C-gehalte kan in diverse producten met verschillende analysemethoden kwantitatief worden bepaald.
- Leerniveau
- HBO; HAVO 5; HBO - Master; VWO 5; HBO - Bachelor;
- Leerinhoud en doelen
- Scheikunde;
- Eindgebruiker
- leraar
- Moeilijkheidsgraad
- gemiddeld
- Trefwoorden
- analysetechnieken, ascorbinezuur, gehalte vitamine c, onderzoeksvaardigheden, reken-/wiskundige vaardigheden, ris-publicatie, ris-publicatie xv, technisch-instrumentele vaardigheden, vitamine