Het arrangement Zuren en basen vmbo is gemaakt met Wikiwijs van Kennisnet. Wikiwijs is hét onderwijsplatform waar je leermiddelen zoekt, maakt en deelt.
- Auteur
- Laatst gewijzigd
- 11-10-2021 14:52:30
- Licentie
-
Dit lesmateriaal is gepubliceerd onder de Creative Commons Naamsvermelding 4.0 Internationale licentie. Dit houdt in dat je onder de voorwaarde van naamsvermelding vrij bent om:
- het werk te delen - te kopiëren, te verspreiden en door te geven via elk medium of bestandsformaat
- het werk te bewerken - te remixen, te veranderen en afgeleide werken te maken
- voor alle doeleinden, inclusief commerciële doeleinden.
Meer informatie over de CC Naamsvermelding 4.0 Internationale licentie.
Aanvullende informatie over dit lesmateriaal
Van dit lesmateriaal is de volgende aanvullende informatie beschikbaar:
- Toelichting
- zuren en basen
- Leerniveau
- VWO 6; VWO 5;
- Leerinhoud en doelen
- Schaal, verhouding en hoeveelheid; Chemische reacties; Scheikunde; Analyse technieken; Reactiviteit; Chemische processen;
- Eindgebruiker
- leerling/student
- Moeilijkheidsgraad
- gemiddeld
- Trefwoorden
- basen, indicator, ph, poh, protonacceptor, protondonor, reacties, titratie, zuren, zuurgraad
Bronnen
| Bron | Type |
|---|---|
|
Rode koolsap als zuur-base-indicator https://youtu.be/4NPFyyLwNG4 |
Video |

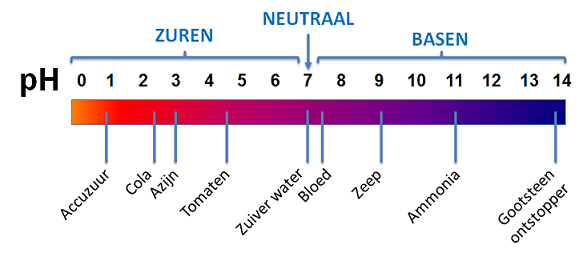
 Je kunt vast wel een aantal stoffen of voedingsmiddelen opnoemen die zuur zijn. Maar deze zijn niet allemaal even zuur. We geven dit aan met de zuurgraad, de pH.
Je kunt vast wel een aantal stoffen of voedingsmiddelen opnoemen die zuur zijn. Maar deze zijn niet allemaal even zuur. We geven dit aan met de zuurgraad, de pH.