Het arrangement Sjakie en zijn spieren is gemaakt met Wikiwijs van Kennisnet. Wikiwijs is hét onderwijsplatform waar je leermiddelen zoekt, maakt en deelt.
- Auteur
- Laatst gewijzigd
- 21-02-2018 15:42:55
- Licentie
-
Dit lesmateriaal is gepubliceerd onder de Creative Commons Naamsvermelding 4.0 Internationale licentie. Dit houdt in dat je onder de voorwaarde van naamsvermelding vrij bent om:
- het werk te delen - te kopiëren, te verspreiden en door te geven via elk medium of bestandsformaat
- het werk te bewerken - te remixen, te veranderen en afgeleide werken te maken
- voor alle doeleinden, inclusief commerciële doeleinden.
Meer informatie over de CC Naamsvermelding 4.0 Internationale licentie.
Aanvullende informatie over dit lesmateriaal
Van dit lesmateriaal is de volgende aanvullende informatie beschikbaar:
- Toelichting
- Practicum voor leerlingen van de Nieuwste School in Tilburg. Deze webquest bestaat uit voorkennis-opdrachten en practicum-opdrachten, die via Google Formulieren worden beantwoord.
- Leerniveau
- VWO 4;
- Leerinhoud en doelen
- Scheikunde; Wereldoriëntatie; Chemisch rekenen;
- Eindgebruiker
- leerling/student
- Moeilijkheidsgraad
- gemiddeld
- Studiebelasting
- 0 uur 50 minuten
Bronnen
| Bron | Type |
|---|---|
|
Sjakie https://www.youtube.com/watch?v=bmWLLempSyI&feature=youtu.be |
Video |
|
Google Formulier Voorkennis opdrachten https://docs.google.com/forms/d/e/1FAIpQLSe9EHmNaBWwjfSPPfEyqnsvOi3GXI0hIv0ZPLx1HNZcs8smSw/viewform?usp=sf_link |
Link |
|
Google Formulier Practicum https://docs.google.com/forms/d/e/1FAIpQLSd6D09sgHfh8wuAGM3g9RR1_7Q_1aj1sKg3VUHs9Z1qsQ58lw/viewform?usp=sf_link |
Link |
|
Titreren http://http://www.hhofstede.nl/nelly/theorie/5VWO/Zuur-base%20titratie.doc |
Link |
Gebruikte Wikiwijs Arrangementen
Dopper, Majoke. (z.d.).
Sjabloon Webquest - kopie








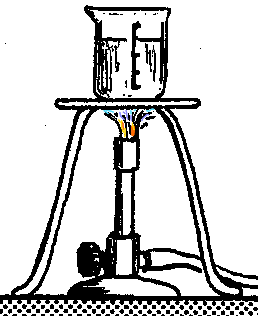

 A indrukken en tegelijkertijd ballon inknijpen.
A indrukken en tegelijkertijd ballon inknijpen.