Het arrangement Klassieke en moderne biotechnologie is gemaakt met Wikiwijs van Kennisnet. Wikiwijs is hét onderwijsplatform waar je leermiddelen zoekt, maakt en deelt.
- Auteur
- Laatst gewijzigd
- 28-04-2021 13:19:53
- Licentie
-
Dit lesmateriaal is gepubliceerd onder de Creative Commons Naamsvermelding-GelijkDelen 4.0 Internationale licentie. Dit houdt in dat je onder de voorwaarde van naamsvermelding en publicatie onder dezelfde licentie vrij bent om:
- het werk te delen - te kopiëren, te verspreiden en door te geven via elk medium of bestandsformaat
- het werk te bewerken - te remixen, te veranderen en afgeleide werken te maken
- voor alle doeleinden, inclusief commerciële doeleinden.
Meer informatie over de CC Naamsvermelding-GelijkDelen 4.0 Internationale licentie.
Aanvullende informatie over dit lesmateriaal
Van dit lesmateriaal is de volgende aanvullende informatie beschikbaar:
- Toelichting
- De Kennisbanken bevatten de theorie bij de opdrachten.
- Leerinhoud en doelen
- Biologie;
- Eindgebruiker
- leerling/student
- Moeilijkheidsgraad
- gemiddeld

 Biotechnologie is het gebruik van biologische systemen voor het maken van producten. Je kunt de klassieke biotechnologie, zoals die al eeuwen lang bestaat, onderscheiden van de moderne biotechnologie. Een voorbeeld van klassieke biotechnologie is het gebruik van gist voor de bereiding van brood of wijn. De moderne biotechnologie past de eigenschappen van bacteriën, planten en dieren voor menselijk gebruik aan, door in te grijpen in het DNA.
Biotechnologie is het gebruik van biologische systemen voor het maken van producten. Je kunt de klassieke biotechnologie, zoals die al eeuwen lang bestaat, onderscheiden van de moderne biotechnologie. Een voorbeeld van klassieke biotechnologie is het gebruik van gist voor de bereiding van brood of wijn. De moderne biotechnologie past de eigenschappen van bacteriën, planten en dieren voor menselijk gebruik aan, door in te grijpen in het DNA. Van het begrip Biotechnologie zijn veel definities in omloop.
Van het begrip Biotechnologie zijn veel definities in omloop.
 Brood verbeteren
Brood verbeteren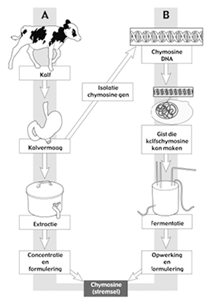 Om kaas te maken moet je de melkeiwitten laten samenklonteren, het zogenaamde stremmen. Dit gebeurt door het toevoegen van een bepaald eiwitsplitsend enzym, chymosine. Vanouds werd dit verkregen uit kalvermagen.
Om kaas te maken moet je de melkeiwitten laten samenklonteren, het zogenaamde stremmen. Dit gebeurt door het toevoegen van een bepaald eiwitsplitsend enzym, chymosine. Vanouds werd dit verkregen uit kalvermagen.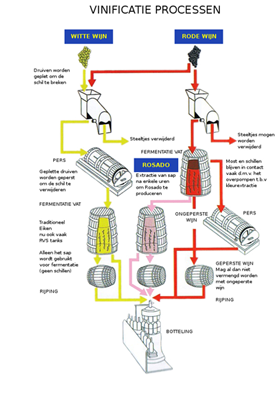 Druivensap bevat suikers die kunnen worden vergist tot alcohol. Bovendien bevat druivensap zuren, zoals wijnsteenzuur en appelzuur. In rijpe druiven is het zuurgehalte lager dan in onrijpe druiven. Als de druiven niet goed rijpen (in een koude zomer) is het zuurgehalte hoger.
Druivensap bevat suikers die kunnen worden vergist tot alcohol. Bovendien bevat druivensap zuren, zoals wijnsteenzuur en appelzuur. In rijpe druiven is het zuurgehalte lager dan in onrijpe druiven. Als de druiven niet goed rijpen (in een koude zomer) is het zuurgehalte hoger. Vlees van landbouwhuisdieren zou je een product van de klassieke biotechnologie kunnen noemen. Door fokken en selecteren zijn de beste vleesrassen ontstaan.
Vlees van landbouwhuisdieren zou je een product van de klassieke biotechnologie kunnen noemen. Door fokken en selecteren zijn de beste vleesrassen ontstaan.

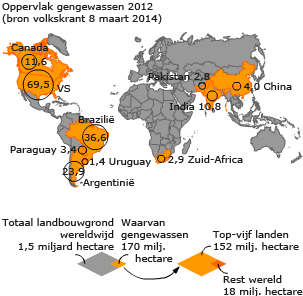 Bij het gebruik van transgene planten is het risico op ziektes die op de mens kunnen worden overgedragen kleiner. Toch blijft het altijd noodzakelijk de producten goed te testen. In soja is bijvoorbeeld een gen gezet uit een Braziliaanse paranoot. Doel was het gehalte aan methionine (een essentieel aminozuur) in de soja te verhogen. Sommige mensen zijn allergisch voor de noot; ze bleken ook allergisch voor de transgene soja.
Bij het gebruik van transgene planten is het risico op ziektes die op de mens kunnen worden overgedragen kleiner. Toch blijft het altijd noodzakelijk de producten goed te testen. In soja is bijvoorbeeld een gen gezet uit een Braziliaanse paranoot. Doel was het gehalte aan methionine (een essentieel aminozuur) in de soja te verhogen. Sommige mensen zijn allergisch voor de noot; ze bleken ook allergisch voor de transgene soja.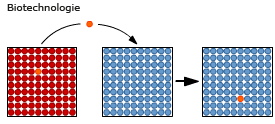

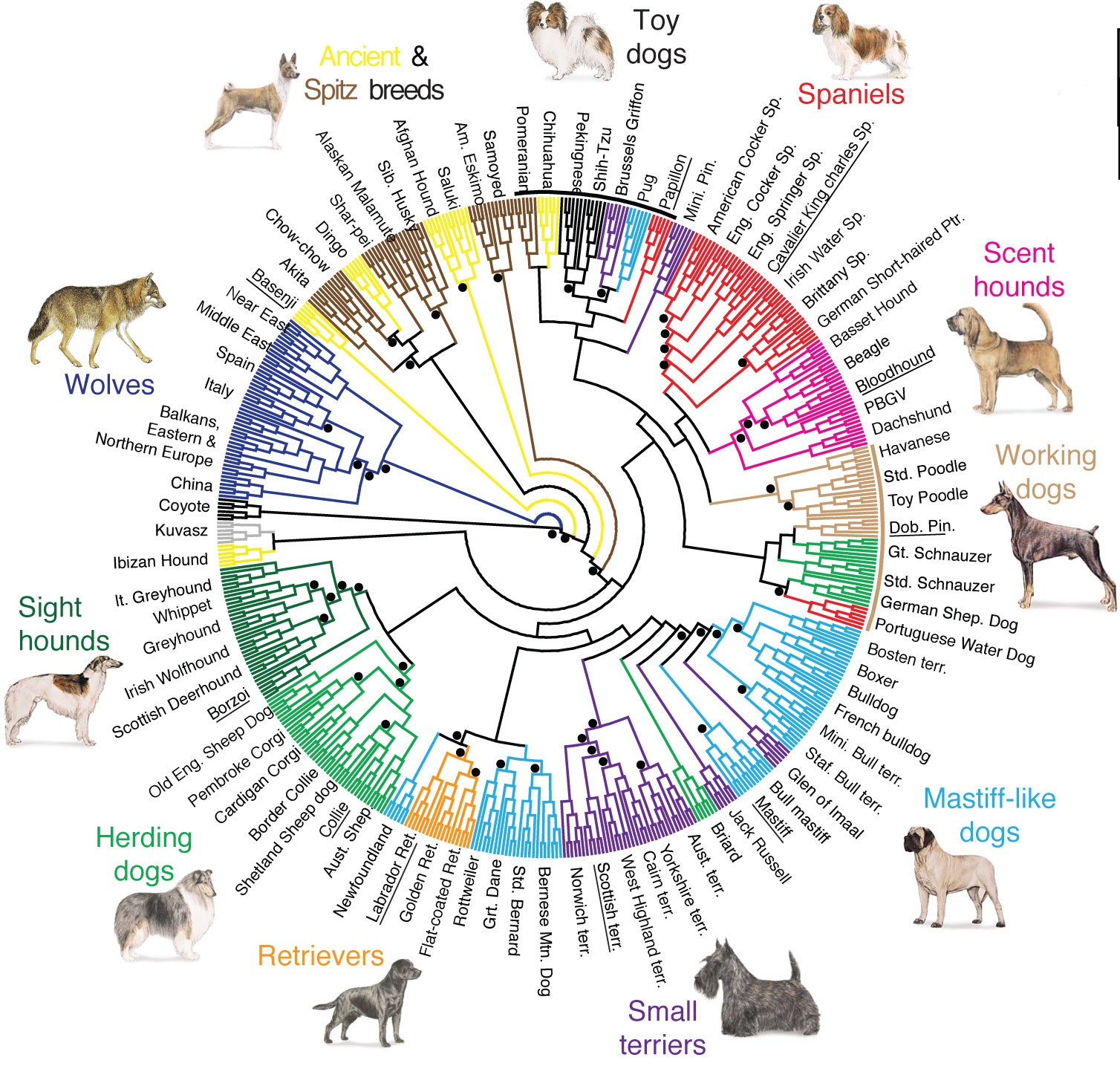
 Rond 1850 fokte Darwin in Londen duiven. Hij ontdekte daarbij het effect van deze kunstmatige selectie, een belangrijke pijler onder zijn latere werk over natuurlijke selectie.
Rond 1850 fokte Darwin in Londen duiven. Hij ontdekte daarbij het effect van deze kunstmatige selectie, een belangrijke pijler onder zijn latere werk over natuurlijke selectie.
 Kunstmatige inseminatie is zeer efficiënt. Tien stieren zijn voldoende om alle koeien in Nederland drachtig te maken. Een nadeel is dat de genetische variatie onder koeien heel klein wordt.
Kunstmatige inseminatie is zeer efficiënt. Tien stieren zijn voldoende om alle koeien in Nederland drachtig te maken. Een nadeel is dat de genetische variatie onder koeien heel klein wordt.