Het arrangement Stoffen en eigenschappen is gemaakt met Wikiwijs van Kennisnet. Wikiwijs is hét onderwijsplatform waar je leermiddelen zoekt, maakt en deelt.
- Auteur
- Laatst gewijzigd
- 27-05-2021 09:35:53
- Licentie
-
Dit lesmateriaal is gepubliceerd onder de Creative Commons Naamsvermelding-GelijkDelen 4.0 Internationale licentie. Dit houdt in dat je onder de voorwaarde van naamsvermelding en publicatie onder dezelfde licentie vrij bent om:
- het werk te delen - te kopiëren, te verspreiden en door te geven via elk medium of bestandsformaat
- het werk te bewerken - te remixen, te veranderen en afgeleide werken te maken
- voor alle doeleinden, inclusief commerciële doeleinden.
Meer informatie over de CC Naamsvermelding-GelijkDelen 4.0 Internationale licentie.
Aanvullende informatie over dit lesmateriaal
Van dit lesmateriaal is de volgende aanvullende informatie beschikbaar:
- Toelichting
- De Kennisbanken bevatten de theorie bij de opdrachten.
- Leerniveau
- VMBO gemengde leerweg, 2; VMBO kaderberoepsgerichte leerweg, 2; VMBO gemengde leerweg, 3; VMBO theoretische leerweg, 4; VMBO theoretische leerweg, 2; VMBO theoretische leerweg, 3; VMBO kaderberoepsgerichte leerweg, 4; VMBO gemengde leerweg, 4; VMBO kaderberoepsgerichte leerweg, 3;
- Leerinhoud en doelen
- Materie; NaSk; Natuurkunde;
- Eindgebruiker
- leerling/student
- Moeilijkheidsgraad
- gemiddeld

 Voorbeelden van stoffen zijn metaal, plastic, glas, katoen, etc.
Voorbeelden van stoffen zijn metaal, plastic, glas, katoen, etc.



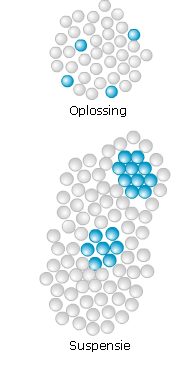 De bouwstenen van stoffen noem je moleculen. Als een stof uit één soort moleculen bestaat, spreek je van een zuivere stof. Zuiver water bestaat uit alleen watermoleculen. 24-karaats goud is ook een voorbeeld van een zuivere stof. Zink, lood en tin zijn metalen die vaak in hun zuivere vorm worden gebruikt.
De bouwstenen van stoffen noem je moleculen. Als een stof uit één soort moleculen bestaat, spreek je van een zuivere stof. Zuiver water bestaat uit alleen watermoleculen. 24-karaats goud is ook een voorbeeld van een zuivere stof. Zink, lood en tin zijn metalen die vaak in hun zuivere vorm worden gebruikt.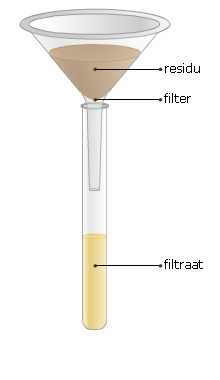 Er zijn verschillende scheidingsmethoden om een mengsel van twee stoffen te scheiden.
Er zijn verschillende scheidingsmethoden om een mengsel van twee stoffen te scheiden.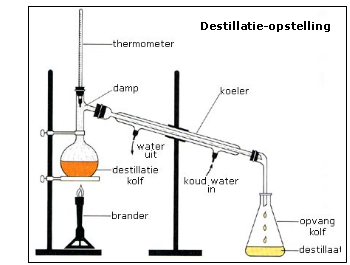 Destilleren
Destilleren