Het arrangement Intro NaSk/ Lj 1-2 / Veiligheid, onderzoek, stoffen en materialen is gemaakt met Wikiwijs van Kennisnet. Wikiwijs is hét onderwijsplatform waar je leermiddelen zoekt, maakt en deelt.
- Auteur
- Laatst gewijzigd
- 03-07-2019 09:36:44
- Licentie
-
Dit lesmateriaal is gepubliceerd onder de Creative Commons Naamsvermelding-GelijkDelen 4.0 Internationale licentie. Dit houdt in dat je onder de voorwaarde van naamsvermelding en publicatie onder dezelfde licentie vrij bent om:
- het werk te delen - te kopiëren, te verspreiden en door te geven via elk medium of bestandsformaat
- het werk te bewerken - te remixen, te veranderen en afgeleide werken te maken
- voor alle doeleinden, inclusief commerciële doeleinden.
Meer informatie over de CC Naamsvermelding-GelijkDelen 4.0 Internationale licentie.
Aanvullende informatie over dit lesmateriaal
Van dit lesmateriaal is de volgende aanvullende informatie beschikbaar:
- Eindgebruiker
- leerling/student
- Moeilijkheidsgraad
- gemiddeld
- Trefwoorden
- arrangeerbaar, leerlijn, rearrangeerbare
Gebruikte Wikiwijs Arrangementen
VO-content M&N. (2022).
Thema: Kijken naar kenmerken - hv123
https://maken.wikiwijs.nl/117897/Thema__Kijken_naar_kenmerken___hv123

 Elke stof is anders
Elke stof is anders
 Opdracht 2 Kenmerkende eigenschappen
Opdracht 2 Kenmerkende eigenschappen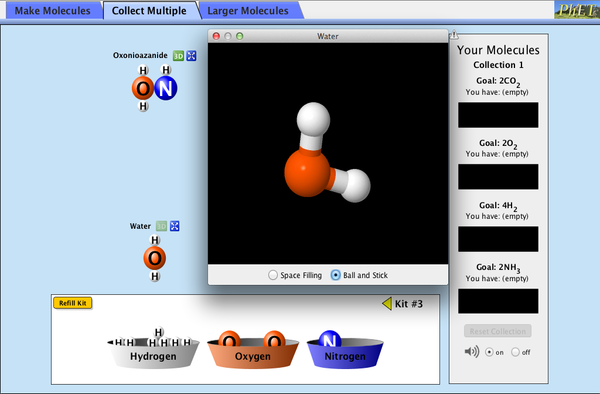




 Opdracht 5 Slagroom en olie en azijn
Opdracht 5 Slagroom en olie en azijn Opdracht 5 Kaarsvet
Opdracht 5 Kaarsvet Opdracht 6* Simulatie
Opdracht 6* Simulatie